Warum einfach, wenn’s auch kompliziert geht?
Es gibt viele verschiedene, sehr unterschiedliche CRISPR-Cas-Systeme
Die verschiedenen CRISPR-Cas-Systeme sind in der Evolution vermutlich mehrfach entstanden. Das heißt, obwohl das Konzept gleich ist, hat die Natur CRISPR-Cas mehrfach unabhängig „erfunden“.
Man kann aber auch davon ausgehen, dass Bakterien einen regen Austausch an genetischer Information über Artgrenzen hinweg machen. Das ist meist kein „nettes, kollegiales“ Verhalten, sondern meist mit Mord, Todschlag und gegenseitiger Ausbeutung verbunden. Aber so können einzelne Gene schon mal von einem Kollegen „ausgeliehen“ werden und man muss nicht alles neu erfinden. Ein gutes Indiz dafür ist auch, dass manche Bakterien gleich mehrere, sehr verschiedene CRISPR-Cas-Systeme haben. Mit größter Wahrscheinlichkeit haben sie die ganze zusätzliche Maschinerie von einem „Bekannten“ geklaut.
Warum sollten sie das tun? Gewiss nicht um anzugeben: schau mal, ich habe zwei Autos und du hast nur eins!
Der Grund liegt wohl eher darin, dass Viren auch nicht „doof“ sind. Sie haben im Laufe der Evolution „anti-CRISPR“-Proteine entwickelt, die das bakterielle Immunsystem ausschalten können. Sie sind dann resistent gegen ein CRISPR-Cas-System – aber eben nicht gegen eins, das ganz anders aussieht!
Inzwischen werden die verschiedenen CRISPR-Cas-Systeme einer von zwei Klassen zugeordnet. Beiden Klassen gemeinsam ist, dass die einzelnen Proteine entsprechend ihren Eigenschaften prinzipiell den vier Funktionen Adaptation, Expression, Interferenz und Signaltransduktion zugeordnet werden könnten.
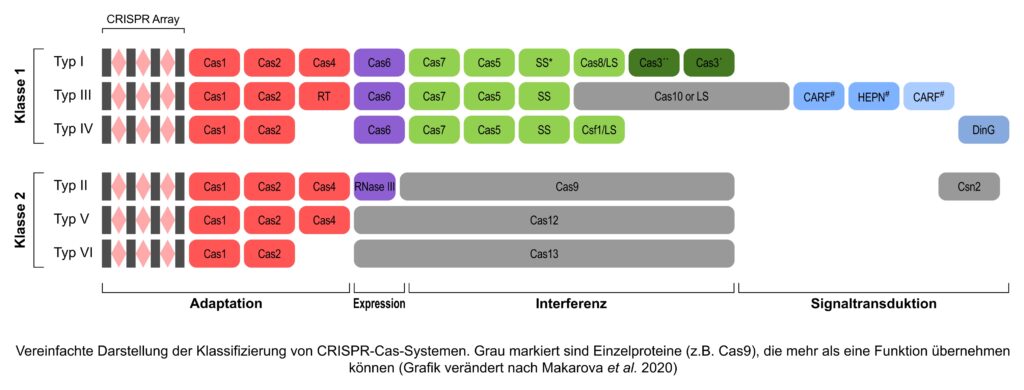
Der entscheidende Unterschied zwischen Klasse 1 und Klasse 2 liegt in der Anzahl an Proteinen, die nötig ist, damit der CRISPR-Komplex an der richtigen Stelle der Zielsequenz binden und diese auch schneiden kann (Expression und Interferenz). Innerhalb der beiden Klassen werden zusätzlich jeweils 3 Typen unterschieden. Während die meisten Typen DNA erkennen und schneiden, haben Typ VI-Systeme RNA als Ziel und Typ III-Systeme können sowohl DNA als auch RNA finden und schneiden. Aber es geht noch weiter: die 6 CRISPR-Typen werden wiederum in 17 Subtypen unterteilt (durch einen Großbuchstaben hinter der römischen Zahl erkennbar, z.B. Typ I-E), die ihrerseits in mehreren Varianten auftreten können (eine Zahl hinter dem Großbuchstaben, z.B. Typ I-E-a) – aber das sei hier nur am Rande erwähnt, um die enorme Vielfalt der CRISPR-Cas-Systeme aufzuzeigen (eine umfassende Übersicht liefert die Arbeit von Makarova et al. 2020).
Wir haben bisher meistens über das DNA schneidende Enzym (Nuklease) Cas9 und ein paar andere CRISPR-Cas-Nukleasen der Klasse 2 gesprochen. Das sind Einzelproteine, die (fast) alles allein können: sie binden die crRNA, erkennen die PAM-Sequenz, finden mit der crRNA die genaue Zielsequenz auf der DNA, binden dort und schneiden beide Stränge der DNA-Doppelhelix. Das ist recht einfach und gut für Anwendungen geeignet. Innerhalb der Klasse 2 unterscheiden sich die Nukleasen aber auch zum Teil gewaltig in ihrer Struktur und ihrer Größe. Zum Beispiel ist Cas-phi (ein erst im Jahr 2020 entdecktes Enzym) mit 70kD (kD = Kilodalton ist eine Masseeinheit für Atome und Moleküle, ein Wasserstoffatom „wiegt“ etwa 1 Dalton) weniger als halb so groß wie Cas9 (158kD; Abb. 1) und kann damit viel leichter in andere Zellen „eingeschmuggelt“ werden.

Die Nukleasen der Klasse 1-Systeme sind dagegen riesig. Wie oben bereits erwähnt, sind die einzelnen Funktionen auf mehrere Proteine verteilt. Diese müssen erst einmal alle ordentlich zusammengesetzt werden, damit die Maschine auch funktioniert. In der nachfolgenden Abb. 2 sieht man, dass der ganze Komplex (hier Typ I aus E. coli) einen „Kopf“ hat, der aus Cas5 und Cse1 besteht und ein Ende aus Cas6e. Dazwischen sitzen sechs Moleküle des Cas7-Proteins, die von zwei Cse2-Molekülen flankiert sind.

Vielleicht kann man ein solches „Monster“ auch im Reagenzglas zusammensetzen, aber das wäre sehr mühsam, zeitaufwändig und teuer. Und es dann funktionsfähig in eine Tier-, Menschen- oder Pflanzenzelle zu kriegen, wäre eine weitere große Herausforderung. Dagegen sind die Enzyme der Klasse 2 ein Kinderspiel. Der Vergleich zwischen den CRISPR-Cas-I- und II-Systemen zeigt, dass eine Aufgabe (hier die Abwehr von Viren) auf sehr unterschiedliche Weise gelöst werden kann. Der Aufwand, den Biolog*innen betreiben müssen, um ein Klasse 1-System nachzubauen, ist sehr groß, ein einfaches Cas9-Protein im Labor zu machen, ist dagegen simpel.
Für Bakterien scheint das keinen Unterschied zu machen. Beide Klassen blieben in der Evolution erhalten und die anscheinend „einfachere“ Lösung der Klasse 2 ist nicht unbedingt besser, weil sie z.B. weniger Energie für die Herstellung braucht. In ihrem Review machen Makarova et al. 2020 zudem deutlich, dass Klasse 1-Systeme (hier vor allem die Typen I und III) innerhalb der Archaeen und Bakterien am häufigsten vorkommen.
Wenn es einem Bakteriophagen gelingt, ein Klasse 2-System „auszutricksen“ und das Abwehrsystem zu umgehen, so wird diese Methode kaum bei einem Klasse 1-System funktionieren: es sieht völlig anders aus, besteht aus ganz anderen Proteinen (was man sich bei der vergleichenden Betrachtung der Abb. 1 und 2 sehr gut vorstellen kann) und arbeitet auch anders – obwohl es denselben Job macht!
Autor: Wolfgang Nellen
Zitierte Literatur: Makarova et al. 2020 und Kuznedelov et al. 2016

